自2019年收购新基以来,百时美施贵宝(BMS)曾连续三年在肿瘤领域位居全球制药巨头榜首。但2023年,BMS丢掉了这一桂冠。
近几年,BMS成熟的抗肿瘤药市场表现进入放缓阶段,血液肿瘤明星药物Revlimid在失去了市场独占权后,去年的销售额下滑了39%;CAR-T疗法Abecma遭遇激烈市场竞争,销售额开始下降;PD-1单抗Opdivo(O药,纳武利尤单抗)在2023年销售额虽然突破了百亿美元,但距离默沙东的Keytruda (帕博利珠单抗,K药)的250亿美元差距甚远。
为寻求肿瘤业务的新增长点,BMS加速布局新型药物,涵盖靶向蛋白降解剂、细胞疗法、核药、抗体偶联药物(ADC)。其中,ADC因其良好的疗效和潜力,成为BMS的重点关注对象。
合作与并购,快速丰富ADC管线
作为ADC赛道的后来者,BMS采取了积极的合作与收购策略。
2021年以来,BMS先后与卫材、Tubulis、Orum公司达成合作,获得了FRα ADC药物MORAb-202、CD33-GSPT1 ADC药物ORM-6151以及P5偶联ADC平台授权。又通过收购Turning Point,获得了礼新医药的CLDN18.2 ADC药物LM-302。2023年12月BMS再次震惊市场,与百利天恒就BL-B01D1达成84亿美元合作,差异化布局双抗ADC赛道。
表1. BMS在ADC领域的交易汇总

资料来源:博药根据企业公开信息整理
MORAb-202
2021年6月,BMS与卫材达成合作,共同开发和商业化FRα ADC产品MORAb-202,BMS支付了6.5亿美元的前期付款、潜在24.5亿美元的里程碑付款。
MORAb-202由卫材研发的FRα抗体farletuzumab和微管抑制剂艾日布林(eribulin)通过组织蛋白酶-B(CathepsinB)可切割接头偶联而成,DAR为4.0。它的独特之处在于有效载荷艾日布林具有多重功能,可以增加ADC旁观者效应。
目前,FRα靶向ADC仅有ImmunoGen公司(已被艾伯维收购)的Elahere(mirvetuximab soravtansine; 索米妥昔单抗)获批上市,治疗FRα高表达、对含铂疗法耐药的经治晚期卵巢癌患者。MORAb-202正在进行临床Ⅱ期研究,适应症包括腹膜癌、输卵管癌、子宫浆液性癌,有望成为FRα赛道的第二款ADC产品。
LM-302
2022年6月,BMS耗资41亿美元收购Turning Point公司,除了获得ROS1靶点明星产品repotrectinib,还将其从礼新药业引进的LM-302(TPX-4589)在除大中华区和韩国外的全球权益也收入囊中。
Claudin 18.2(CLDN 18.2) 在胃癌等消化道肿瘤中高表达或异位激活,被视为抗肿瘤的新兴靶标。2024年3月,安斯泰来的Zolbetuximab(IMAB362)在日本批准上市,成为全球首款获批上市的 Claudin 18.2 抗体。但目前尚无CLDN 18.2靶向ADC药物获批上市。
LM-302是一款Claudin 18.2靶向ADC药物,由礼新医药基于独家多次跨膜蛋白抗体发现平台开发的Claudin 18.2 特异性抗体、可裂解连接子,以及毒素载荷甲基澳瑞他汀 E(MMAE)组成。目前该药已启动 Ⅲ期临床试验,用于治疗 CLDN18.2 阳性局部晚期或转移性胃及胃食管结合部腺癌,处于Claudin 18.2靶向ADC赛道第一梯队。
ORM-6151
2023年11月,BMS与Orum公司达成合作,引进一款在研潜在“first-in-class”抗体偶联蛋白质降解剂项目ORM-6151,BMS支付1亿美元预付款、总交易金额1.8亿美元。
根据BMS新闻稿,该药已获FDA批准开展治疗急性髓性白血病或高危骨髓增生异常综合症的1期临床。
P5偶联ADC平台
除了单品引进,BMS还与Tubulis达成ADC技术平台合作。
2023年4月,BMS向Tubulis支付2275万美元首付款、超10亿美元潜在里程碑付款,获得对Tubulis的专有P5偶联平台和Tubutecan技术平台的独家访问权,以开发预定数量针对实体瘤的高度差异化ADCs。
根据Tubulis官网介绍,公司开发了一套互补的技术平台,用于发现和开发新一代的多功能且可定制的抗体-药物偶联物(ADCs)
其P5偶联ADC技术平台可以快速生成兼具稳定性和化学灵活性连接子的ADC,为开发真正差异化抗体偶联药物提供了机会:
·均一性的DAR8偶联比例
·化学灵活性和广泛的ADC设计可能性
·新型半胱氨酸选择性化学方法
·独特的稳定性和选择性
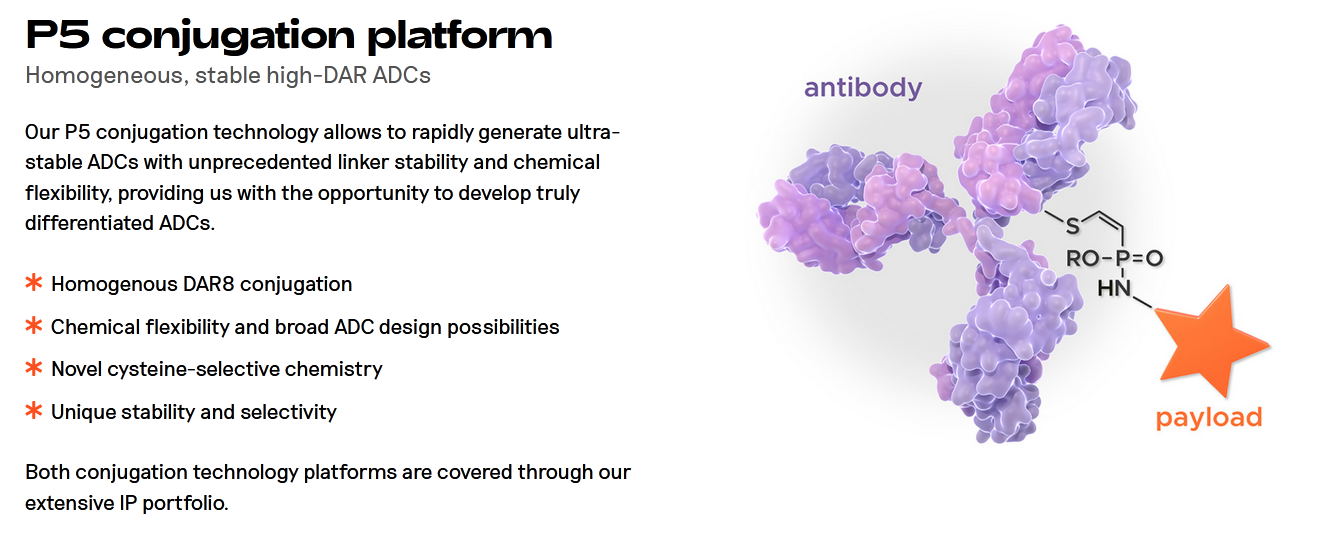
图片来源:Tubulis公司官网
BMS通过与Tubulis的合作,有望借助其技术平台的优势,赋能管线、靶点、适应症的快速扩张,实现弯道超车。
84亿美元,在双抗ADC领域抢得先机
BMS虽然在ADC领域进行了多项交易,但比起其他布局ADC多年且已有产品上市的制药巨头,BMS作为后来者,还需要更多差异化的管线。
2023年12月,BMS与国内药企百利天恒子公司SystImmune达成了84亿美元总额的BD交易,首付款8亿美元,获得一款EGFR/HER3双靶点ADC药物BL-B01D1。这笔交易不仅创下国内创新药License-out交易的首付款纪录,也一举刷新了全球ADC单药交易总价纪录。
根据协议,双方将在美国联合开发并商业化 BL-B01D1;SystImmune保留中国大陆的独家权益,而百时美施贵宝将获得在全球其他市场的独家许可。
相较于单抗ADC,双抗ADC具有诸多优点:既能通过双靶点增强细胞杀伤毒性,克服耐药性,又能增强肿瘤细胞特异性,减少副作用,而且双抗ADC产生新的结合和内吞动力学机制,能达到更好的治疗效果。
目前全球尚无双抗ADC获批上市,进入临床阶段的也不过十余个,进展最快的是百利天恒的BL-B01D1和康宁杰瑞的JSKN003。
表2. 部分全球在研ADC项目
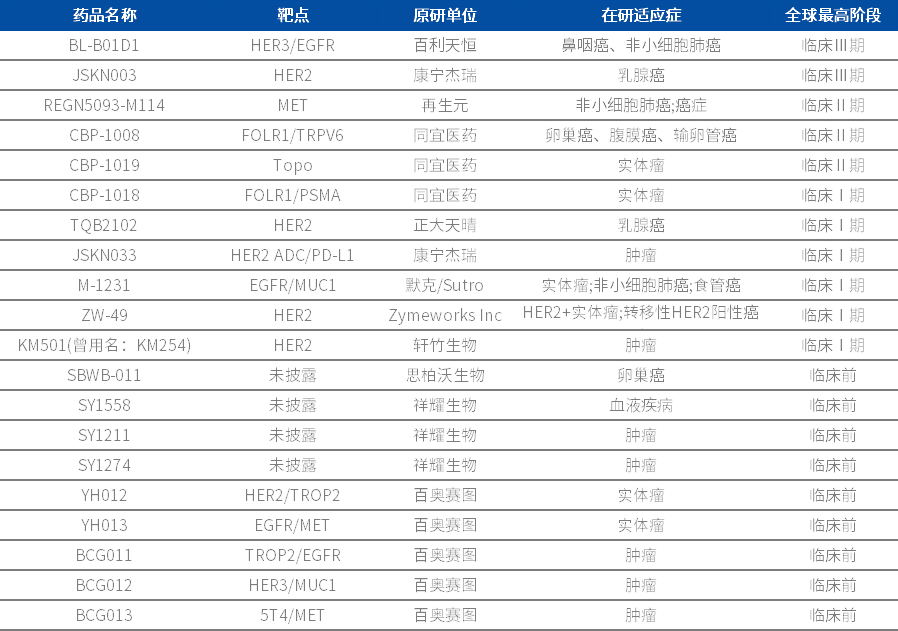
数据来源:药智数据
BL-B01D1是一款潜在的同类首创EGFRxHER3双抗ADC,其抗体部分采用了百利天恒自研的EGFR/HER3双抗SI-B001,小分子毒素部分是自研的喜树碱衍生物Ed-04,并采用AClinker将Ed-04连接到抗体的半胱氨酸位点,DAR值为8,不仅具有旁观者效应,在预防HER3引起的耐药性的同时,还可以针对EGFR依赖肿瘤靶向杀伤。
目前BL-B01D1单药已在国内开展了5个Ia/Ib期临床研究,覆盖16种肿瘤,其中鼻咽癌适应症已处于临床Ⅲ期阶段,非小细胞肺癌适应症处于临床Ⅰ期试验。
在美国,BL-B01D1于2023年7月1日获得美国FDA的批准开展用于治疗复发和难治型非小细胞肺癌的临床试验。
在2023ESMO大会上百利天恒公布了BL-B01D1治疗非小细胞肺癌患者的I期研究结果:在经过大量前线治疗的NSCLC,特别是EGFRmutNSCLC中表现出良好的疗效,观察到的毒性被认为是可接受的。
BMS重金押注BL-B01D1,一举成为双抗ADC赛道的领军者。而且BL-B01D1还有与其PD-1抑制剂O药联用的潜力,进一步扩大其在肿瘤治疗领域的影响力。
结语
在ADC赛道,尽管BMS公司起步较晚,但凭借其积极的合作与收购策略,迅速崛起,如今已拥有多个处于临床阶段的ADC药物管线。而且BMS差异化地布局了新一代ADC技术平台和双抗ADC,展现出后来者居上的潜力。
加之BMS在肿瘤治疗领域深厚的研发与临床经验积累,使其能够精准把握市场需求,有望给ADC领域带来新突破,也为肿瘤患者带来了新的治疗选择。




合作咨询
![]() 肖女士
肖女士 ![]() 021-33392297
021-33392297 ![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2024 上海博华国际展览有限公司版权所有(保留一切权利) 黑ICP备32063282号-1
2006-2024 上海博华国际展览有限公司版权所有(保留一切权利) 黑ICP备32063282号-1